유기체의 70~90%를 구성하는 물은 생물의 탄생과 진화에 있어서 필수적으로 다뤄야 하는 물질이라고 할 수 있습니다. 일반화학과 유기화학을 열심히 공부했다는 가정 하에, 생화학 수준에서 물에 대해 알아보겠습니다.
- 물의 구조(Structure of water)
물의 화학식은 H2O 이고 입체 구조는 다음과 같습니다.
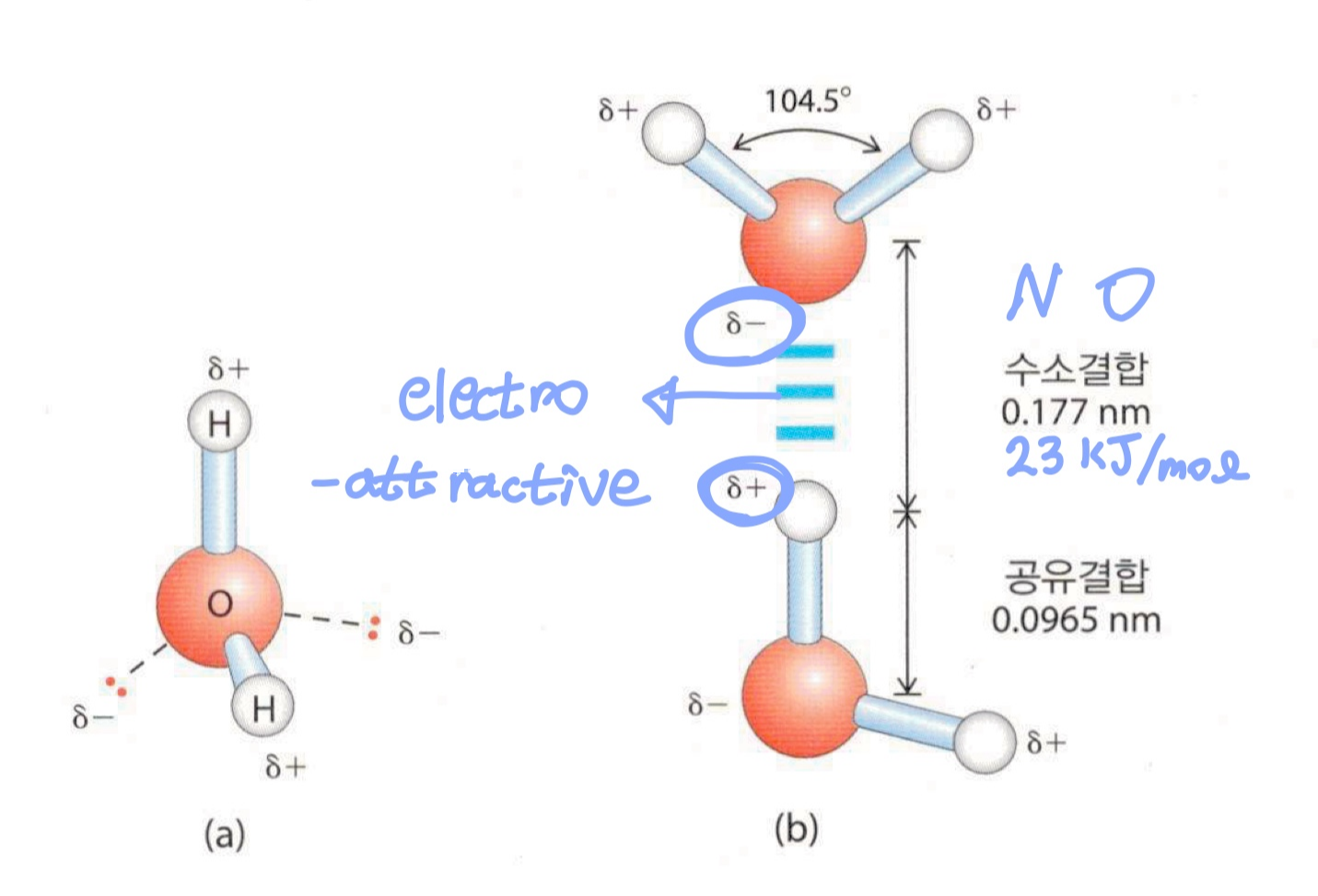
물은 O 하나에 H 2개가 결합한 형태로로써 전자가 sp3 오비탈 4개로 존재하여 2개의 오비탈은 H+와 결합하고, 2개의 오비탈은 결합하지 않은 형태인 lone pair(고립 전자쌍)로 존재합니다. 이러한 형태를 기하학적으로 didtorted tetrahedron, 왜곡된 사면체라고 부르며 흔히 일반화학이나 고등화학에서는 비교적 lone pair을 고려하지 않는 표현인 굽은형이라고 칭합니다. O와 H의 전기 음성도 차이가 크기 때문에-O의 원자핵 H의 원자핵보다 강하게 전자를 끌어당기므로-O는 전자쌍을 끌어당겨 상대적으로 음전하를 띠고, H는 상대적으로 양전하를 띱니다. 이에 따라 물 분자는 dipole moment(쌍극자 모멘트)를 가져 후에 기술할 수소 결합에서의 수용자와 기부자 역할을 모두 수행할 수 있습니다.
- 수소 결합(Hydrogen Bond)
물의 가장 중요한 특징은 대부분의 다른 용매보다 비정상적으로 끓는점, 녹는점, 기화열, 표면장력이 높다는 것입니다. 이는 물 분자 간의 단순한 분자 간 인력을 제외하고도 강한 내부 응집력을 갖게 해주는 결합이 있기 때문인데요, 물의 구조 부분에서 설명하였듯 물 분자 내에서 O와 H 는 각각 양전하와 음전하를 띠어, 물 분자의 O 원자와 다른 물 분자의 H 원자 사이에 정전기적 인력이 발생합니다. 이러한 정전기적 인력으로 인해 생기는 결합을 수소 결합이라고 합니다. 위 그림의 (b)에서 볼 수 있듯 공유결합보다는 결합 거리가 멀기 때문에 수소 결합의 결합력 또한 공유 결합보단 약합니다. 물에서 H-O 결합의 결합 에너지가 420KJ/mol이고, 수소결합 에너지가 23KJ/mol 인 것을 생각하면 대략 20배 정도 약하다고 생각하면 될 것 같습니다.
이와 같이 물에서 발견할 수 있는 수소 결합은 비단 물에만 존재하는 것이 아니라 우리 몸의 아주 다양한 곳에서 매우 중요한 역할을 합니다. 아래 그림에도 나와 있지만, 몇가지 예를 들자면 수소 결합은 단백질, DNA, 다당류의 구조와 기능을 결정하는 데에 그리고 효소와 기질, 호르몬과 수용체의 결합에 중요하게 작용합니다. 즉 수소 결합은 어떤 전기음성원자-일반적으로 O나 N-와, 다른 분자에 있는 전기음성도가 큰 원자에 공유결합을 이룬 H 원자 사이에서 쉽게 형성됩니다. 다만 C는 상대적으로 전기음성도가 크지 않기 때문에 C-H 결합은 대부분의 상황에서 수소 결합 형성에 관여하지 않고, 극히 약한 극성을 가집니다.
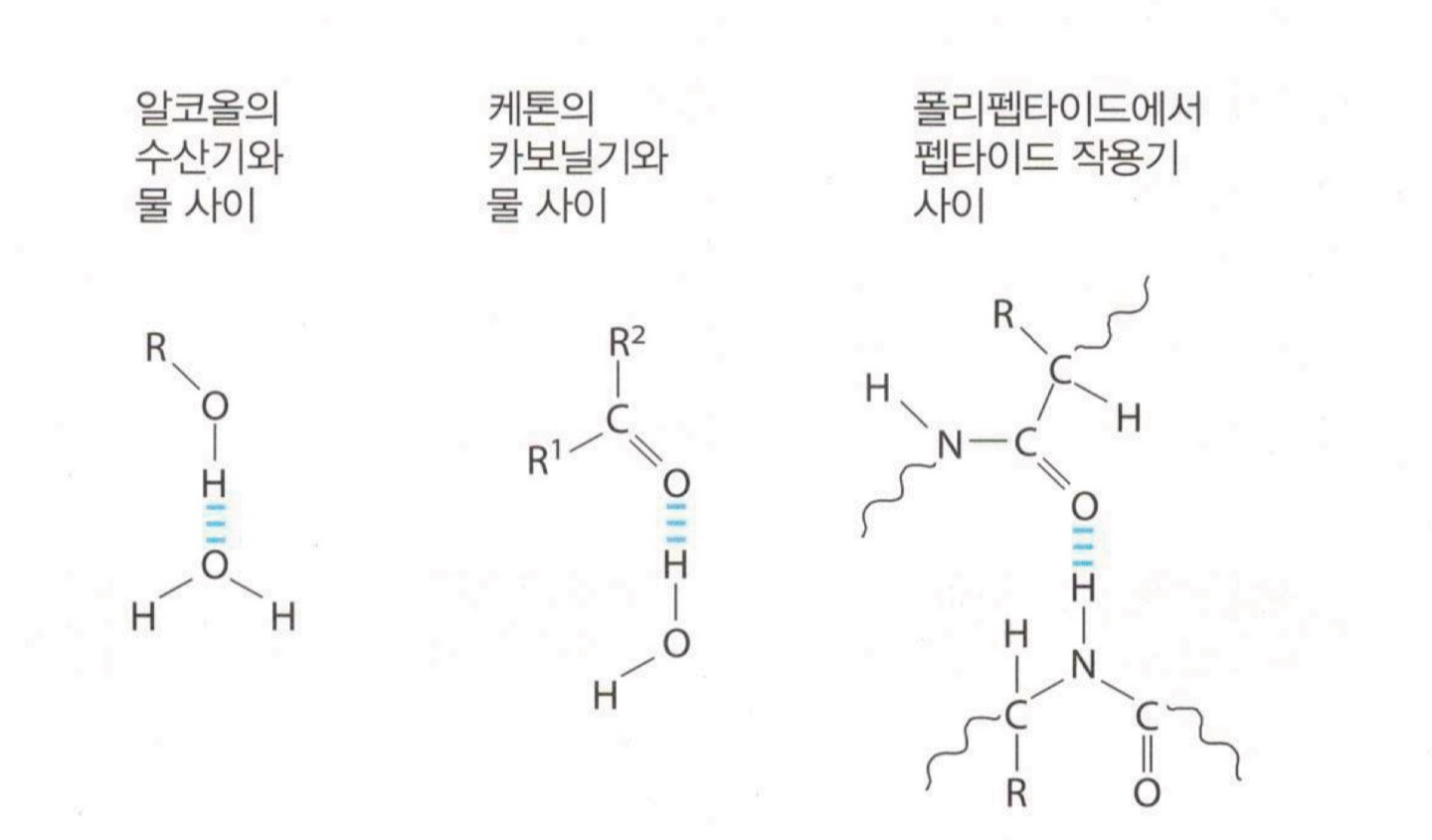
수소 결합은 결합된 분자들 간에 정전기적 인력이 최대가 되도록 놓여 있을 때, 즉 H 원자와 그것을 공유한 2개의 원자가 직선상에 있을 때에 제일 강해집니다. 이와 같은 배열은 H+ 이온의 양전하가 직접 두 개의 부분적 음전하 간에 놓이는 형태라고 할 수 있죠.

이와 같이 수소결합은 방향성을 띠며, 2개의 수소결합으로 된 분자 또는 기능기를 어떠한 기하학적인 위치로 고정할 수 있게 합니다. 이는 수소결합을 많이 갖는 단백질과 핵산이 매우 정교한 3차원 구조를 이룰 수 있는 이유이기도 합니다.
- 얼음: 물의 고체 상태
물은 많은 결정 형태(crystal forms)를 가지고 있지만 육각형태의 얼음(hexagonal ice)이 가장 일반적인 형태입니다. 물의 구조 파트에서 서술했듯 물은 정사면체에 가까운 구조이기 때문에 이론적으로 각 물 분자는 인접해 있는 물 분자 4개와 수소 결합을 할 수 있습니다. 하지만 액체상의 물은 흐르기 때문에-계속해서 파괴되고 연속적으로 운동하므로- 어떠한 한 순간에 물 분자는 3.4개의 물 분자와 수소결합을 형성한다고 합니다. 하지만 고체 형태인 얼음에서는 물 분자들이 고정돼 있기 때문에, 4개의 다른 물 분자와 수소결합을 형성하여 일정한 형태로 격자 구조(lattice)를 형성합니다. 이러한 격자 구조 때문에 육각 얼음은 낮은 엔트로피를 갖고, 액체 상태의 물보다 낮은 밀도를 가지며, 얼음이 물에 뜨게 되는 것이죠. 아래 그림은 hexagonal ice의 격자 형태를 보여줍니다.

-용매로서의 물 (Water as a Solvent)
물은 위에서 살펴보았듯, dipole moment 를 띠기 때문에 극성 용매입니다. 따라서 용매로서 '물'은 생체 분자 중에서도 전하를 가지거나 극성을 띠는 화합물을 쉽게 용해시킵니다. 물에 쉽게 녹는 화합물을 친수성(hydrophillic)이라 하고, 물에 쉽게 녹지 않는 화합물을 소수성(hydrophobic)이라고 합니다. 위 두 용어는 교재에서도, 교수님께서도 자주 사용하지만 발음이 비슷해 헷갈리는 경우가 많으니 외우면 좋습니다. 물과는 대조적으로 벤젠이나 클로로폼과 같은 비극성 용매는 지질이나 왁스 같은 소수성의 생체 분자를 쉽게 녹입니다. 대표적으로 친수성인(극성을 띠는) 생체 분자는 아미노산, 펩타이드, 분자량이 작은 알코올, 탄수화물이 있고, 소수성인(비극성인) 생체 분자는 비극성 가스(기체), 방향성(aromatic) 부분, 지방성(aliphatic) 부분이 있습니다. 다음 표에서 생체 분자들이 왜 친수성 혹은 소수성을 띠는지 알 수 있습니다.
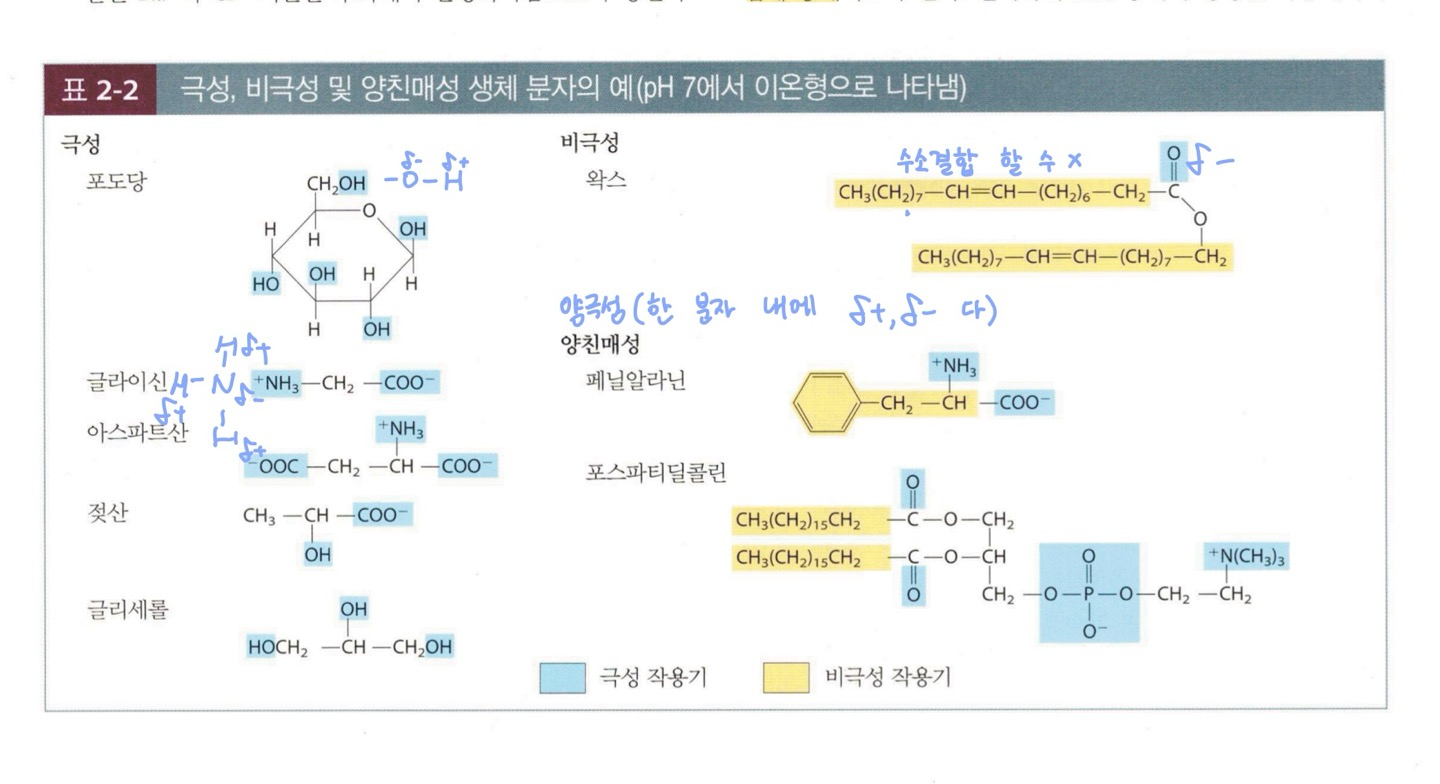
- 양친매성(amphipathic) 화합물과 소수성 상호작용(hydrophobic interactions)
바로 위 Table에서 나온 양친매성 화합물은 극성 영역과 비극성 영역을 모두 가진 화합물을 의미합니다. 이 화합물이 물에 녹을 때 극성 영역은 hydrophillic 하므로 용해되려 하고 비극성 영역은 hydrophobic 하여 물과 접촉을 피하려 하게 됩니다. 따라서 분자의 비극성 영역은 물을 피라기 위해 서로 뭉치고, 극성 영역이 물과의 상호작용을 하기 위해 바깥쪽으로 배열돼 구와 같은 형태를 이루게 됩니다. 이러한 물속에서 양친매성 화합물의 안정한 구조를 micelle 이라 부르고, 분자의 비극성(소수성) 영역을 결합시키는 힘을 소수성 상호작용 이라고 부릅니다. 이는 양친매성 화합물의 소수성 부분이 주위의 물 분자를 정렬시켜 발생하는 엔트로피의 감소를 최소화시켜 반응계를 안정시키기 위해 생기는 힘입니다.


- 반데르발스 상호작용 (van der waals interaction)
반데르발스 상호작용은 원자 간의 작용하는 매우 약한 인력입니다. 이는 흔히 분산력(Rondon dispersion force) 형태로 나타나는 힘입니다. 하나의 분자 또는 핵 근처의 무작위한 변동이 일시적으로 쌍극자를 형성시키고, 근처에 있는 원자에서 일시적으로 반재방향의 쌍극자가 유도되는데, 이 2개의 쌍극자 간에 생기는 일시적인 인력을 반데르발스 결합이라고 합니다. 이 인력으로 인해 2개의 핵이 가까워지다가도 일정 거리 이상으로 가까워지면 서로의 전자가 반발하기 시작하는데, 이 인력과 반발력이 평형을 이루는 지점이 생깁니다. 이 평형을 이루는 지점을 반데르발스 반지름이라 부르고 이는 어떠한 원자가 다른 원자에 접근하는 것을 허용하는 거리라고 할 수 있습니다. 사실 생화학에서는 이러한 힘이 있다는 정도만 알면 되긴 합니다.
- 비공유결합성 상호작용 (noncovalent interactions)
이제 오늘의 마지막 소주제입니다. 생화학에서 공유결합보다 훨씬 더 많은 역할을 담당하는 비공유결합성 상호작용입니다. 지금까지 위에서 알아보았던 수소결합, 소수성 상호작용, 반데르발스 상호작용, 그리고 이온결합을 통틀어 비공유결합성 상호작용이라고 칭하는데요, 수소결합 부분에서 살펴보았듯 이들은 공유결합과는 비교도 안될 정도로 약한 수준의 결합력을 가지고 있습니다. 또 하나의 예시로 C-H 1몰의 단일 공유결합을 파괴하는 데에는 410KJ 이 필요하지만 1몰의 반데르발스 상호작용을 파괴하는 데에는 4KJ 밖에 들지 않습니다. 하지만 이 4가지 형태의 결합은 공유결합보다 결합 위력은 약하지만 인체에서 그 수가 매우 많기 때문에 단백질이나 핵산에 구조와 기능에 지대한 영향을 미칩니다. 예를 들어보면 효소와 기질의 비공유결합은 수소결합, 반데르발스 상호작용, 이온 상호작용을 무조건 가지고 있습니다. 효소와 기질의 결합과 같이 다수의 약한 비공유적으로 결합된 2개의 분자를 해리하려면 많은 결합이 동시에 파괴되어야 하는데, 그 수가 많기 때문에 동시적인 파괴는 거의 불가능합니다. 따라서 5~20개의 약한 상호작용에 의해 생기는 분자간의 결합 안정성이 엄청나케 크다고 할 수 있습니다.
이들은 분자 간 결합의 안정성 뿐만 아니라 구조에도 크게 관여합니다. DNA, RNA 나 단백질과 같은 거대 분자는 이 noncovalent interactions이 발생하는 자리를 많이 가지게 되므로 이들의 가장 안정한 구조는 이 약한 결합이 최대한 많이 생길 수 있는 구조가 됩니다. 긴 단일 폴리펩타이드나 폴리뉴클레오타이드 사슬들이 3차원의 단백질, DNA 로 접히는 것이 바로 이러한 약한 결합의 작용으로 인한 것입니다.


'생화학' 카테고리의 다른 글
| [생화학] 0. 생화학 개관 (1) | 2024.09.06 |
|---|
